Cyswllt:Cyfeiliorn Zhou (Mr.)
Ffôn: plws 86-551-65523315
Symudol/WhatsApp: plws 86 17705606359
CQ:196299583
Skype:lucytoday@hotmail.com
E-bost:sales@homesunshinepharma.com
Ychwanegu:1002, Huanmao Adeilad, Rhif 105, Mengcheng Ffordd, Hefei Dinas, 230061, Tsieina
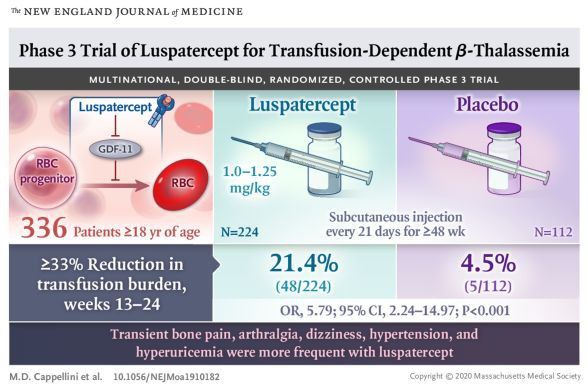
Yn ddiweddar, mae Bristol-Myers Squibb (BMS) ac Acceleron Pharmaceuticals wedi cyhoeddi bod canlyniadau astudiaeth BELIEVE cam allweddol III sy'n gwerthuso'r asiant aeddfedu celloedd gwaed coch Reblozyl (luspatercept) wrth drin beta thalassemia wedi'u cyhoeddi yn y cyfnodolyn meddygol rhyngwladol gorau" New England Journal of Medicine" (NEJM)). Teitl yr erthygl yw: Treial Cyfnod 3 o Luspatercept mewn Cleifion â β-Thalassemia Trallwysiad-Ddibynnol.
Dangosodd y canlyniadau fod gan gleifion yn y grŵp triniaeth Reblozyl faich sylweddol is o drallwysiad gwaed o gymharu â'r grŵp plasebo. Yn seiliedig ar ganlyniadau'r astudiaeth hon, cymeradwywyd Reblozyl gan FDA yr UD ym mis Tachwedd 2019 ar gyfer trin anemia mewn cleifion sy'n oedolion â beta thalassemia sy'n gofyn am drwythiad celloedd gwaed coch rheolaidd.
Reblozyl yw'r cyffur cyntaf a gymeradwywyd gan FDA i drin anemia beta sy'n gysylltiedig â thalassemia, a hwn yw'r asiant aeddfedu celloedd gwaed coch cyntaf a'r unig gymeradwyaeth gan FDA, sy'n cynrychioli dosbarth newydd o therapi sy'n helpu cleifion i leihau celloedd gwaed coch trwy reoleiddio'r cam hwyr. aeddfedu celloedd gwaed coch Baich trwyth. Dylid nodi nad yw Reblozyl yn addas yn lle trwyth celloedd gwaed coch mewn cleifion sydd angen cywiro anemia ar unwaith.
Mae BELIEVE yn astudiaeth aml-fenter ar hap, dwbl-ddall, a reolir gan placebo, a gynhelir mewn cleifion sy'n oedolion â β-thalassemia sy'n ddibynnol ar drallwysiad ac sydd angen trallwysiad celloedd gwaed coch rheolaidd (6-20 uned o drallwysiad celloedd gwaed coch bob 24 wythnos , Ac yn ystod y cyfnod hwn, nid oes unrhyw gyfnod trallwysiad gwaed yn fwy na 35 diwrnod). Yn yr astudiaeth, neilltuwyd cleifion ar hap i dderbyn Reblozyl wedi'i gyfuno â'r driniaeth gefnogol orau (BSC) neu blasebo mewn cyfuniad â BSC. Yn yr astudiaeth hon, roedd BSC yn cynnwys: trwyth celloedd gwaed coch, cyffuriau chelating haearn, gwrthfiotigau, cyffuriau gwrthfeirysol, triniaeth gwrthffyngol, a / neu gymorth maethol yn ôl yr angen.
Dangosodd y canlyniadau, yn ystod y 1 {{1 3}} - {{1 5}} 4 wythnos, bod cyfran y cleifion y gostyngwyd eu baich trallwysiad celloedd gwaed coch gan> ; {{1}}% (o leiaf {{{{1 5}}}} uned) o'r lefel waelodlin yn sylweddol uwch yn y grŵp triniaeth Reblozyl na'r grŵp plasebo, gan gyrraedd yr astudiaeth.&# {{{{1 3}}}}; s prif ddiweddbwynt. Yn ogystal, cyflawnodd yr astudiaeth yr holl bwyntiau terfyn eilaidd allweddol: cleifion â gostyngiad yn y baich trallwysiad erythrocyte> {{1}}% yn ystod wythnosau {{1 3}} {{{{ 1 4}}}} - 49, cleifion â gostyngiad yn y baich trallwysiad erythrocyte> {{{{1 {{2 2}}}}} }% yn ystod wythnosau 1 {{1 3}} - {{1 5}} 4 neu {{1 3}} {{{{{19} } 4}}}} - 4 {{2 1}} Yn gymesur, roedd y grŵp triniaeth Reblozyl yn sylweddol uwch na'r grŵp plasebo. Yn yr astudiaeth hon, roedd y digwyddiadau niweidiol mwyaf cyffredin (unrhyw radd) yn y grŵp triniaeth Reblozyl fwy na 5% yn uwch na'r rhai yn y grŵp plasebo: poen esgyrn ({{1 0}}. { {{{1 4}}}}% vs {{1 {{1 5}}}}. {{1 3}}%), pendro ( {{1 4}}. {{1 5}}% vs {{1 {{1 {{2 2} }}}}}. {{1 {{2 2}}}}%), a gorbwysedd ({{1 {{1 5 }}}}. 1% vs {{1 5}}. {{2 1}}%), hyperuricemia ({{{{1 4}} }}. {{1 5}}% o'i gymharu â 0%).
Cynhwysyn fferyllol gweithredol Reblozyl' s yw luspatercept, sy'n asiant aeddfedu celloedd gwaed coch o'r radd flaenaf (EMA) sy'n rheoleiddio aeddfedu celloedd gwaed coch hwyr. Mae'r cyffur yn brotein ymasiad hydawdd. Mae parth Fc IgG dynol 1 wedi'i asio â pharth allgellog derbynnydd math activin IIB (ActRIIB). Fel trap ligand, gall reoleiddio aeddfedu RBC hwyr trwy rwymo wedi'i dargedu. Mae ligand penodol y ffactor twf trawsnewidiol (TGF) -β superfamily yn lleihau actifadu'r llwybr signalau Smad 2 / 3 , yn gwella cynhyrchu celloedd gwaed coch aneffeithiol, yn hyrwyddo aeddfedu gwaed coch hwyr celloedd, ac yn cynyddu lefelau haemoglobin.
Datblygwyd Luspatercept yn fyd-eang gan Shinki (a gafwyd gan BMS) mewn cydweithrediad ag Acceleron Pharmaceuticals. Ar hyn o bryd, mae'r partïon hefyd yn gwerthuso potensial luspatercept ar gyfer trin asiantau ysgogol erythropoiesis (ESA), cleifion MDS risg isel (astudiaeth Cam III COMMANDS), thalassemia beta di-drallwysiad (astudiaeth Cam II BEYOND), a myelofibrosis. Mae'r diwydiant hefyd yn optimistaidd iawn ynghylch rhagolygon busnes Luspatercept' s. Ddiwedd y llynedd, rhyddhaodd EvaluatePharma yr adroddiad" Vantage 2019 Preview", a oedd yn cyfrif yr 20 mwyaf gwerthfawr R& D prosiectau yn y byd. Safleodd Luspatercept 18 th gyda gwerth presennol net (NPV) o US $ 3. 1 biliwn.

Ar hyn o bryd, mae Reblozyl' s cais arall am drwydded bioleg (BLA) ar gyfer trin syndrom myelodysplastig (MDS) yn cael ei adolygu gan yr FDA ar hyn o bryd. RS) ac mae angen trwyth o gelloedd coch y gwaed (RBC) ar gyfer cleifion sy'n anemia cysylltiedig â syndrom myelodysplastig risg isel i risg gymedrol (MDS). Dyddiad targed dull ffioedd defnyddiwr cyffuriau presgripsiwn (PDUFA) yw Ebrill 4, 2020.
Yn gynharach, nododd dadansoddwyr o fanc buddsoddi enwog Wall Street, Jefferies, os bydd anemia syndrom myelodysplastig (MDS) hefyd yn cael ei gymeradwyo gan yr FDA, bydd brig gwerthiant blynyddol Reblozyl' s yn cyrraedd 2 biliwn yr UD. doleri.