Cyswllt:Cyfeiliorn Zhou (Mr.)
Ffôn: plws 86-551-65523315
Symudol/WhatsApp: plws 86 17705606359
CQ:196299583
Skype:lucytoday@hotmail.com
E-bost:sales@homesunshinepharma.com
Ychwanegu:1002, Huanmao Adeilad, Rhif 105, Mengcheng Ffordd, Hefei Dinas, 230061, Tsieina
Mae Myovant Sciences yn gwmni gofal iechyd sy'n canolbwyntio ar ailddiffinio gofal menywod a dynion. Yn ddiweddar, cyhoeddodd y cwmni fod Asiantaeth Meddyginiaethau Ewrop (EMA) wedi derbyn cais am awdurdodiad marchnata (MAA) ar gyfer ail-leoli ar gyfer trin canser datblygedig y prostad a bydd yn cychwyn ar broses adolygu ffurfiol.
Mae Relugolix yn antagonist derbynnydd hormon rhyddhau gonadotropin llafar (GnRH) sy'n atal cynhyrchu testosteron yn y testes, hormon sy'n ysgogi twf celloedd canser y prostad. Yn ogystal, gall relugolix hefyd leihau cynhyrchiad estradiol ofarïaidd trwy rwystro derbynyddion GnRH yn y chwarren bitwidol. Gwyddys bod yr hormon hwn yn ysgogi twf ffibroidau groth ac endometriosis.
Un o'r opsiynau triniaeth confensiynol ar gyfer canser datblygedig y prostad yw therapi amddifadedd androgen (ADT), sy'n defnyddio cyffuriau i leihau lefel yr hormonau sy'n helpu celloedd canser y prostad i dyfu. Ar hyn o bryd, pigiad neu fewnblaniad isgroenol yw ADT a ddefnyddir yn glinigol. Os caiff ei gymeradwyo, relugolix fydd yr ADT llafar cyntaf a'r unig ADT llafar ar gyfer canser datblygedig y prostad yn Ewrop.
Ym mis Rhagfyr 2020, cymeradwywyd relugolix gan FDA yr UD ar gyfer trin cleifion sy'n oedolion â chanser datblygedig y prostad. Cafodd y cyffur ei farchnata o dan yr enw brand Orgovyx (relugolix, tabledi 120mg). Mae'n werth nodi mai Orgovyx yw'r ADT llafar cyntaf a'r unig ADT a gymeradwywyd gan FDA yr UD ar gyfer trin canser datblygedig y prostad, yn ogystal â'r antagonydd derbynnydd GnRH llafar cyntaf a'r unig un. cymeradwywyd relugolix trwy'r broses adolygu blaenoriaeth. Yn astudiaeth Cam III HERO, roedd cyfradd dileu triniaeth relugolix mor uchel â 96.7%, a oedd yn sylweddol well nag asetad leuprolide (88.8%), gan leihau'r risg o ddigwyddiadau niweidiol cardiofasgwlaidd mawr (MACE) 54%.
Yn ôl telerau datblygu cydweithredol Myovant a Pfizer' s a masnacheiddio relugolix, mae gan Pfizer yr hawl i fasnacheiddio relugolix ym maes oncoleg y tu allan i'r Unol Daleithiau a Chanada (ac eithrio rhai gwledydd Asiaidd). Os yw Pfizer yn arfer yr opsiwn hwn, bydd Myovant yn derbyn $ 50 miliwn ac yn gymwys i dderbyn breindaliadau dau ddigid o werthiannau net yn y marchnadoedd hyn. Disgwylir i benderfyniad Pfizer' s i arfer yr opsiwn hwn gael ei wneud yn hanner cyntaf 2021.
Dywedodd David Marek, Prif Swyddog Gweithredol y Gwyddorau Myovant:" Rydym yn falch iawn bod Asiantaeth Meddyginiaethau Ewrop wedi derbyn y cais am awdurdodiad marchnata ar gyfer relugolix i'w adolygu. Mae hon yn garreg filltir bwysig a fydd yn dod â photensial i gleifion datblygedig canser y prostad yn Ewrop. Opsiynau triniaeth geg. Yn dilyn cymeradwyaeth a rhestriad diweddar yr FDA yn yr Unol Daleithiau, credwn fod gan relugolix y potensial i newid safon y gofal ar gyfer cleifion canser datblygedig y prostad sydd angen therapi amddifadedd androgen. Rydym yn edrych ymlaen at ddarparu hyn i fwy o gleifion gwrywaidd ledled y byd Opsiwn triniaeth bosibl. Quot GG;
Mae cais rheoliadol Relugolix' s ar gyfer trin canser datblygedig y prostad yn seiliedig ar ganlyniadau cadarnhaol astudiaeth HERO Cam III. Mae hwn yn astudiaeth glinigol ar hap, label agored, grŵp cyfochrog, astudiaeth glinigol aml-wlad sy'n cymharu relugolix ac asetad leuprolide. Mewn mwy na 900 o achosion, roedd sensitifrwydd androgen triniaeth amddifadedd androgen (ADT) yn gofyn am o leiaf blwyddyn. Wedi'i gynnal mewn cleifion â chanser datblygedig y prostad. Yn yr astudiaeth, neilltuwyd cleifion ar hap ar gymhareb 2: 1 a chawsant relugolix (dos llwytho sengl 360 mg, ac yna 120 mg unwaith y dydd) neu bigiadau ataliad depo asetad leuprolide (unwaith ym mis Mawrth).
Dangosodd y canlyniadau fod relugolix wedi cyrraedd y pwynt terfyn effeithiolrwydd sylfaenol: cyflawnodd 96.7% o ddynion yn y grŵp relugolix ataliad testosteron parhaus ar y lefel ysbaddu (GG lt; 50ng / dL) yn ystod 48 wythnos o driniaeth, tra bod cyfran y grŵp triniaeth asetad leuprolide yn oedd 88.8%. Yn ogystal, cyrhaeddodd relugolix bob un o'r 6 phwynt terfyn eilaidd allweddol (pob gwerth p< 0.0001),="" gan="" ddangos="" ei="" fod="" yn="" well="" nag="" asetad="" leuprolide="" o="" ran="" atal="" testosteron="" yn="" gyflym="" ac="" yn="" ddwfn,="" ymateb="" psa,="" ac="" adferiad="" testosteron="" ar="" ôl="" rhoi'r="" gorau="" i="" driniaeth.="" roedd="" cyfanswm="" yr="" achosion="" o="" ddigwyddiadau="" niweidiol="" yn="" y="" grŵp="" relugolix="" a'r="" grŵp="" asetad="" leuprolide="" yn="" gymharol="" (92.9%="" o'i="" gymharu="" â="" 93.5%).="" o="" ran="" digwyddiadau="" cardiofasgwlaidd="" niweidiol="" mawr="" (mace),="" roedd="" risg="" y="" grŵp="" relugolix="" 54%="" yn="" is="" na="" risg="" y="" grŵp="" asetad="" leuprolide="" (cyfradd="" mynychder:="" 2.9%="" o'i="" gymharu="" â="" 6.2%).="" roedd="" y="" digwyddiadau="" hyn="" yn="" cynnwys="" cnawdnychiant="" myocardaidd="" angheuol,="" strôc="" angheuol="" a="" pawb="" oherwydd="" marwolaeth.="" ymhlith="" dynion="" â="" hanes="" o="" mace,="" bu="" gostyngiad="" o="" 80%="" yn="" adroddiadau="" digwyddiadau="" mace="" yn="" y="" grŵp="" relugolix="" o="" gymharu="" â'r="" grŵp="" asetad="" leuprolide="" (3.6%="" o'i="" gymharu="" â="" 17.8%).="" mae="" gan="" ddiweddbwynt="" eilaidd="" arall="" o="" ran="" goroesi="" heb="" wrthwynebiad="" ysbaddu,="" relugolix="" ac="" asetad="" leuprolide="" gyfraddau="" goroesi="" tebyg="" heb="" wrthwynebiad="" ysbaddu="" yn="" yr="" is-grŵp="" gwrywaidd="" o="" glefyd="" metastatig="" (74%="" o'i="" gymharu="" â="" 75%),="" na="" chyrhaeddodd="" arwyddocâd="" ystadegol.="" y="" fantais="" (p="">
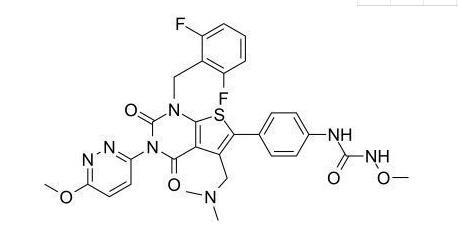
Strwythur cemegol Relugolix (ffynhonnell: medchemexpress.com)
datblygwyd relugolix gan Takeda, a chafodd Myovant Sciences (cwmni a ffurfiwyd gan Roivant a Takeda) y drwydded fyd-eang unigryw ym mis Mehefin 2016 ac eithrio Japan a gwledydd Asiaidd eraill. Yn Japan, cymeradwywyd relugolix ym mis Ionawr 2019 a'i farchnata o dan yr enw brand Relumina i wella'r symptomau canlynol a achosir gan ffibroidau groth: menorrhagia, poen yn yr abdomen is, poen yng ngwaelod y cefn ac anemia.
Yn yr Unol Daleithiau, canser y prostad yw'r ail ganser blaenllaw mewn dynion a'r ail brif achos marwolaeth o ganser mewn dynion. Marwolaeth gardiofasgwlaidd yw prif achos marwolaeth mewn dynion â chanser y prostad, gan gyfrif am 34% o farwolaethau mewn dynion â chanser y prostad. Mae canser datblygedig y prostad yn cyfeirio at ganser y prostad sydd wedi lledu neu ail-adrodd ar ôl triniaeth, a gall gynnwys dynion ag ailddigwyddiad biocemegol (codiadau PSA pan nad oes clefyd metastatig ar ddelweddu), clefyd datblygedig lleol neu glefyd metastatig. Mae trin canser datblygedig y prostad fel arfer yn cynnwys therapi amddifadedd androgen (ADT), sy'n lleihau testosteron i lefelau isel iawn, y cyfeirir atynt yn gyffredin fel lefelau ysbaddu. Ar hyn o bryd, agonyddion derbynnydd hormonau sy'n rhyddhau gonadotropin (GnRH), fel asetad leuprolide neu bigiadau rhyddhau parhaus, yw safon y gofal ar gyfer therapi amddifadedd androgen (ADT). Fodd bynnag, gall agonyddion derbynnydd GnRH fod yn gysylltiedig â chyfyngiadau mecanwaith, gan gynnwys codiadau cychwynnol a allai fod yn niweidiol mewn lefelau testosteron, a allai waethygu symptomau clinigol (hy fflerau clinigol neu hormonaidd), ac oedi adferiad testosteron ar ôl terfynu.